درمان سرطان سینه در ترکیه
لامپکتومی Lumpectomy
ماستکتومی Mastectomy
بیوپسی غدد لنفاوی سمینال Sentinel lymph node biopsy.
جراحی ترمیمی (پلاستیک).

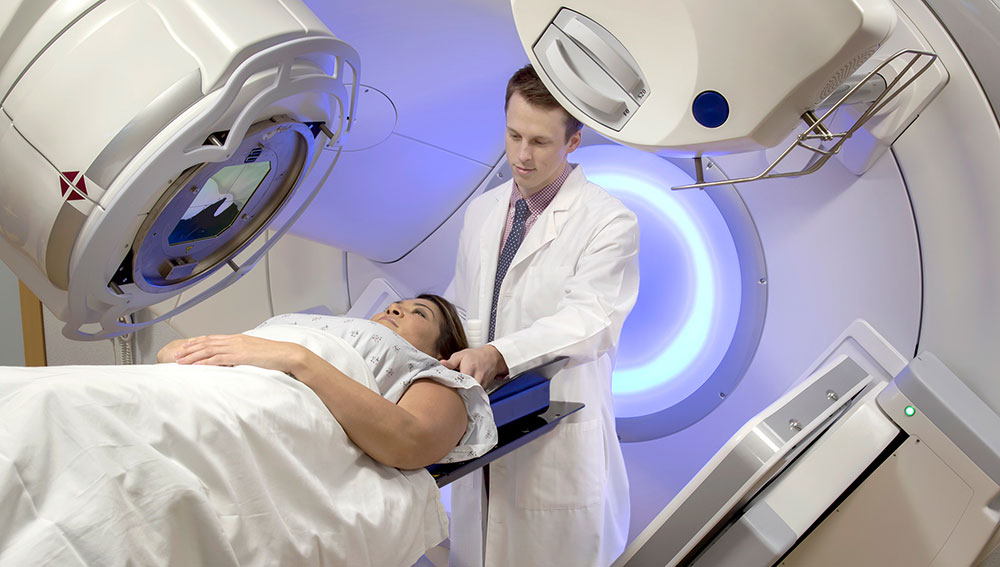
پرتو درمانی
Radiation therapy is usually given daily for a set number of weeks.
- After a lumpectomy.Radiation therapy after a lumpectomy is external-beam radiation therapy given Monday through Friday for 3 to 4 weeks if the cancer is not in the lymph nodes. If the cancer is in the lymph nodes, radiation therapy is given for 5 to 6 weeks. However, this duration is changing, as there is a preference for a shorter duration to be given in women who meet the criteria for shorter treatment. This often starts with radiation therapy to the whole breast, followed by a more focused treatment to where the tumor was located in the breast for the remaining treatments.
This focused part of the treatment, called a boost, is standard for women with invasive breast cancer to reduce the risk of a recurrence in the breast. Women with DCIS may also receive the boost. For women with a low risk of recurrence, the boost may be optional. It is important to discuss this treatment approach with your doctor.
- After a mastectomy.For those who need radiation therapy after a mastectomy, it is usually given 5 days a week for 5 to 6 weeks. Radiation therapy can be given before or after reconstructive surgery. As is the case following lumpectomy, some women may be recommended to have less than 5 weeks of radiation therapy after mastectomy.
Even shorter schedules have been studied and are in use in some centers, including accelerated partial breast radiation therapy (see below) for 5 days.
These shorter schedules may not be options for women who need radiation therapy after a mastectomy or radiation therapy to their lymph nodes. Also, longer schedules of radiation therapy may be needed for some women with very large breasts.
- Partial breast irradiation.Partial breast irradiation (PBI) is radiation therapy that is given directly to the tumor area instead of the entire breast. It is more common after a lumpectomy. Targeting radiation directly to the tumor area usually shortens the amount of time that patients need to receive radiation therapy. However, only some patients may be able to have PBI. Although early results have been promising, PBI is still being studied. However, it is already part of routine care in certain circumstances, including for specific people with early-stage breast cancer. You may want to discuss with your radiation oncologist the pros and cons of PBI compared to whole breast radiation therapy.
PBI can be done with standard external-beam radiation therapy that is focused on the area where the tumor was removed and not on the entire breast. PBI may also be done with brachytherapy by using plastic catheters or a metal wand placed temporarily in the breast. Breast brachytherapy can involve short treatment times, ranging from 1 dose to 1 week. It can also be given as 1 dose in the operating room immediately after the tumor is removed. These forms of focused radiation therapy are currently used only for patients with a smaller, less aggressive, and lymph node-negative tumor.
- Intensity-modulated radiation therapy.Intensity-modulated radiation therapy (IMRT) is a more advanced way to give external-beam radiation therapy to the breast. The intensity of the radiation directed at the breast is varied to better target the tumor, spreading the radiation more evenly throughout the breast. The use of IMRT lessens the radiation dose and may decrease possible damage to nearby organs, such as the heart and lung, as well as lessen the risks of some immediate side effects, such as peeling of the skin during treatment. This can be especially important for women with medium to large breasts who have a higher risk of side effects, such as peeling and burns, compared with women with smaller breasts. IMRT may also help to lessen the long-term effects on the breast tissue, such as hardness, swelling, or discoloration, that were common with older radiation techniques.
IMRT is not recommended for everyone. Talk with your radiation oncologist to learn more. Special insurance approval may also be needed for coverage for IMRT. It is important to check with your health insurance company before any treatment begins to make sure it is covered.
- Proton therapy.Standard radiation therapy for breast cancer uses x-rays, also called photon therapy, to kill cancer cells. Proton therapy is a type of external-beam radiation therapy that uses protons rather than x-rays. At high energy, protons can destroy cancer cells. Protons have different physical properties that may allow the radiation therapy to be more targeted than photon therapy and potentially reduce the radiation dose. The therapy may also reduce the amount of radiation that goes near the heart. Researchers are studying the benefits of proton therapy versus photon therapy in a national clinical trial. Currently, proton therapy is an experimental treatment and may not be widely available or covered by health insurance.
برنامه پرتودرمانی
پرتودرمانی معمولاً روزانه به مدت چند هفته انجام می شود.
Adjuvant radiation therapy concerns for older patients and/or those with a small tumor
Recent research studies have looked at the possibility of avoiding radiation therapy for women age 65 or older with an ER-positive, lymph node-negative, early-stage tumor (see Introduction), or for women with a small tumor. Importantly, these studies show that for women with small, less aggressive breast tumors that are removed with lumpectomy, the likelihood of cancer returning in the same breast is very low. Treatment with radiation therapy reduces the risk of breast cancer recurrence in the same breast even further compared with surgery alone. However, radiation therapy does not lengthen women’s lives.
Guidelines from the National Comprehensive Cancer Network (NCCN) continue to recommend radiation therapy as the standard option after lumpectomy. However, they note that women with special situations or a low-risk tumor could reasonably choose not to have radiation therapy and use only systemic therapy (see below) after lumpectomy. This includes women age 70 or older, as well as those with medical conditions that could limit life expectancy within 5 years. People who choose this option will have a modest increase in the risk of the cancer coming back in the breast. It is important for these women to discuss the pros and cons of omitting radiation therapy with their doctor.
Therapies using medication (updated 01/2021)
Systemic therapy is the use of medication to destroy cancer cells. Medications circulate through the body and therefore can reach cancer cells throughout the body. Systemic therapies are generally prescribed by a medical oncologist, a doctor who specializes in treating cancer with medication.
Common ways to give systemic therapies include an intravenous (IV) tube placed into a vein using a needle, an injection into a muscle or under the skin, or in a pill or capsule that is swallowed (orally).
The types of systemic therapies used for breast cancer include:
- Chemotherapy
- Hormonal therapy
- Targeted therapy
- Immunotherapy
Each of these therapies is discussed below in more detail. A person may receive 1 type of systemic therapy at a time or a combination of systemic therapies given at the same time. They can also be given as part of a treatment plan that includes surgery and/or radiation therapy. The medications used to treat cancer are continually being evaluated. Your doctor may suggest that you consider participating in clinical trials that are studying new ways to treat breast cancer.
Talking with your doctor is often the best way to learn about the medications that can be prescribed for you, their purposes, and their potential side effects. It is also important to let your doctor know if you are taking any other prescription or over-the-counter medications or supplements. Herbs, supplements, and other drugs can interact with cancer medications. Learn more about your prescriptions by using searchable drug databases.
- شیمی درمانی
- درمان هورمونی
- درمان هدفمند
- ایمونوتراپی
Chemotherapy is the use of drugs to destroy cancer cells, usually by keeping the cancer cells from growing, dividing, and making more cells. It may be given before surgery to shrink a large tumor, make surgery easier, and/or reduce the risk of recurrence, called neoadjuvant chemotherapy. It may also be given after surgery to reduce the risk of recurrence, called adjuvant chemotherapy.
A chemotherapy regimen, or schedule, usually consists of a combination of drugs given in a specific number of cycles over a set period of time. Chemotherapy may be given on many different schedules depending on what worked best in clinical trials for that specific type of regimen. It may be given once a week, once every 2 weeks, once every 3 weeks, or even once every 4 weeks. There are many types of chemotherapy used to treat breast cancer. Common drugs include:
- Docetaxel (Taxotere)
- Paclitaxel (Taxol)
- Doxorubicin (available as a generic drug)
- Epirubicin (Ellence)
- Pegylated liposomal doxorubicin (Doxil)
- Capecitabine (Xeloda)
- Carboplatin (available as a generic drug)
- Cisplatin (available as a generic drug)
- Cyclophosphamide (available as a generic drug)
- Eribulin (Halaven)
- Fluorouracil (5-FU)
- Gemcitabine (Gemzar)
- Ixabepilone (Ixempra)
- Methotrexate (Rheumatrex, Trexall)
- Protein-bound paclitaxel (Abraxane)
- Vinorelbine (Navelbine)
A patient may receive 1 drug at a time or a combination of different drugs given at the same time. Research has shown that combinations of certain drugs are sometimes more effective than single drugs for adjuvant treatment. ASCO does not recommend routinely adding platinum chemotherapy (cisplatin or carboplatin) to anthracycline (doxorubicin or epiribicin) or taxane (paclitaxel or docetaxel) chemotherapy to treat people with inherited BRCA mutations before or after surgery.
The following drugs or combinations of drugs may be used as adjuvant therapy for early-stage and locally advanced breast cancer:
- AC (doxorubicin and cyclophosphamide)
- EC (epirubicin, cyclophosphamide)
- AC or EC followed by T (paclitaxel or docetaxel), or the reverse)
- CAF (cyclophosphamide, doxorubicin, and 5-FU)
- CEF (cyclophosphamide, epirubicin, and 5-FU)
- CMF (cyclophosphamide, methotrexate, and 5-FU)
- TAC (docetaxel, doxorubicin, and cyclophosphamide)
- TC (docetaxel and cyclophosphamide)
Therapies that target the HER2 receptor may be given with chemotherapy for HER2-positive breast cancer (see "Targeted therapy," below). An example is the antibody trastuzumab. Combination regimens for early-stage HER2-positive breast cancer may include:
- AC-TH (doxorubicin, cyclophosphamide, paclitaxel or docetaxel, trastuzumab)
- AC-THP (doxorubicin, cyclophosphamide, paclitaxel or docetaxel, trastuzumab, pertuzumab)
- TCH (paclitaxel or docetaxel, carboplatin, trastuzumab)
- TCHP (paclitaxel or docetaxel, carboplatin, trastuzumab, pertuzumab)
- TH (paclitaxel, trastuzumab)
The side effects of chemotherapy depend on the individual, the drug(s) used, whether the chemotherapy has been combined with other drugs, and the schedule and dose used. These side effects can include fatigue, risk of infection, nausea and vomiting, hair loss, loss of appetite, diarrhea, constipation, numbness and tingling, pain, early menopause, weight gain, and chemo-brain or cognitive dysfunction. These side effects can often be very successfully prevented or managed during treatment with supportive medications, and they usually go away after treatment is finished. For hair loss reduction, talk with your doctor about whether they do cold cap techniques. Rarely, long-term side effects may occur, such as heart damage, permanent nerve damage, or secondary cancers such as leukemia or lymphoma.
Many patients feel well during chemotherapy and are actively taking care of their families, working, and exercising during treatment, although each person’s experience can be different. Talk with your health care team about the possible side effects of your specific chemotherapy plan, and seek medical attention immediately if you experience a fever during chemotherapy.
Learn more about the basics of chemotherapy.
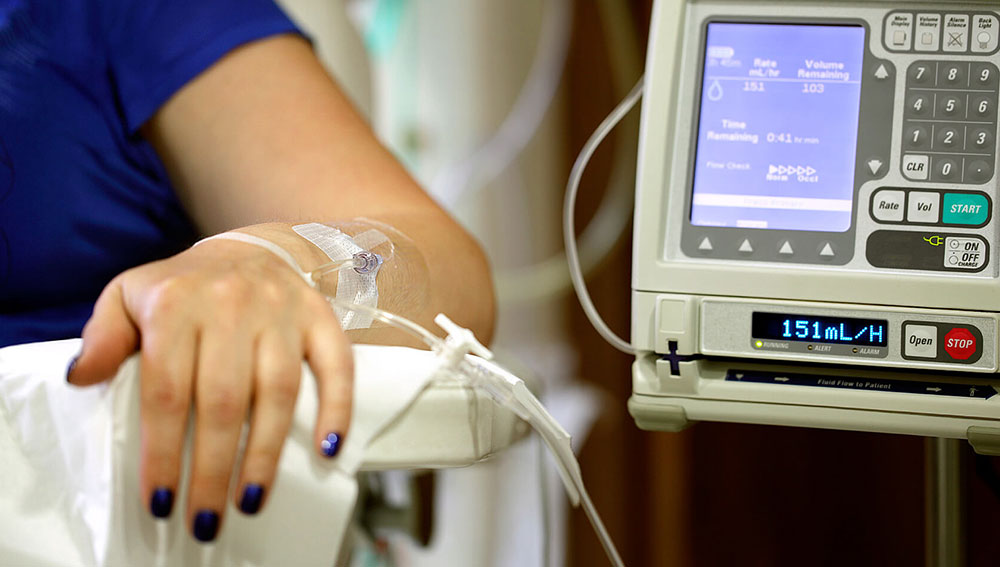
شیمی درمانی
- دوستاکسل (Taxotere)
- پاکلیتاکسل (تاکسول)
- دوکسوروبیسین (موجود به عنوان یک داروی ژنریک)
- اپی روبیسین (Ellence)
- دوکسوروبیسین لیپوزومی پگیله (دوکسیل)
- کاپسیتابین (Xeloda)
- کربوپلاتین (موجود به عنوان یک داروی ژنریک)
- سیس پلاتین (موجود به عنوان یک داروی ژنریک)
- سیکلوفسفامید (موجود به عنوان یک داروی ژنریک)
- اریبولین (هالاون)
- فلوئورواوراسیل (5-FU)
- جمسیتابین (جمزار)
- Ixabepilone (Ixempra)
- متوترکسات (روماترکس، ترکسال)
- پاکلی تاکسل متصل به پروتئین (آبراکسان)
- Vinorelbine (Navelbine)
- AC (دوکسوروبیسین و سیکلوفسفامید)
- EC (اپی روبیسین، سیکلوفسفامید)
- AC یا EC و به دنبال آن T (پاکلیتاکسل یا دوستاکسل)، یا برعکس)
- CAF (سیکلوفسفامید، دوکسوروبیسین و 5-FU)
- CEF (سیکلوفسفامید، اپی روبیسین و 5-FU)
- CMF (سیکلوفسفامید، متوترکسات و 5-FU)
- TAC (دوستاکسل، دوکسوروبیسین و سیکلوفسفامید)
- TC (دوستاکسل و سیکلوفسفامید)
- AC-TH (دوکسوروبیسین، سیکلوفسفامید، پاکلیتاکسل یا دوستاکسل، تراستوزوماب)
- AC-THP (دوکسوروبیسین، سیکلوفسفامید، پاکلیتاکسل یا دوستاکسل، تراستوزوماب، پرتوزوماب)
- TCH (پاکلیتاکسل یا دوستاکسل، کربوپلاتین، تراستوزوماب)
- TCHP (پاکلیتاکسل یا دوستاکسل، کربوپلاتین، تراستوزوماب، پرتوزوماب)
- TH (پاکلیتاکسل، تراستوزوماب)
Hormonal therapy, also called endocrine therapy, is an effective treatment for most tumors that test positive for either estrogen or progesterone receptors (called ER positive or PR positive; see Introduction). This type of tumor uses hormones to fuel its growth. Blocking the hormones can help prevent a cancer recurrence and death from breast cancer when hormonal therapy is used either by itself or after chemotherapy.
Hormonal therapy for breast cancer treatment is different than menopausal hormone therapy (MHT). MHT may also be called postmenopausal hormone therapy or hormone replacement therapy (HRT). Hormonal therapies used in breast cancer treatment act as “anti-hormone” or “anti-estrogen” therapies. They block hormone actions or lower hormone levels in the body. Hormonal therapy may also be called endocrine therapy. The endocrine system in the body makes hormones.
Hormonal therapy may be given before surgery to shrink a tumor, make surgery easier, and/or lower the risk of recurrence. This is called neoadjuvant hormonal therapy. When given before surgery, it is typically given for at least 3 to 6 months before surgery and continued after surgery. It may also be given solely after surgery to reduce the risk of recurrence. This is called adjuvant hormonal therapy.
Types of hormonal therapy
- Tamoxifen is a drug that blocks estrogen from binding to breast cancer cells. It is effective for lowering the risk of recurrence in the breast that had cancer, the risk of developing cancer in the other breast, and the risk of distant recurrence. Tamoxifen works in women who have been through menopause as well as those who have not.
Tamoxifen is a pill that is taken daily by mouth every day for 5 to 10 years. For premenopausal women, it may be combined with medication to stop the ovaries from producing estrogen. It is important to discuss any other medications or supplements you take with your doctor, particularly any anti-depression medications, as there are some that may interfere with tamoxifen. Common side effects of tamoxifen include hot flashes and vaginal dryness, discharge, or bleeding. Very rare risks include a cancer of the lining of the uterus, cataracts, and blood clots. However, tamoxifen may improve bone health and cholesterol levels.
- Aromatase inhibitors (AIs).AIs decrease the amount of estrogen made in tissues other than the ovaries in post-menopausal women by blocking the aromatase enzyme. This enzyme changes weak male hormones called androgens into estrogen when the ovaries have stopped making estrogen during menopause. These drugs include anastrozole (Arimidex), exemestane (Aromasin), and letrozole (Femara). All of the AIs are pills taken daily by mouth. Only women who have gone through menopause or who take medicines to stop the ovaries from making estrogen (see "Ovarian suppression," below) can take AIs. Treatment with AIs, either as the first hormonal therapy taken or after treatment with tamoxifen, may be more effective than taking only tamoxifen to reduce the risk of recurrence in post-menopausal women. Post-menopausal women with hormone receptor-positive breast cancer can:
- Begin hormone therapy with an AI. When an AI is the only hormone therapy given, it’s taken for 5 to 10 years.
- Begin hormone therapy with tamoxifen and then after a few years, switch to an AI. When an AI is taken after tamoxifen, the drugs are taken for a combined total of 5 to 10 years.
درمان هورمونی
انواع هورمون درمانی
- . The side effects of AIs may include muscle and joint pain, hot flashes, vaginal dryness, an increased risk of osteoporosis and broken bones, and rarely, increased cholesterol levels and thinning of hair. Research shows that all AIs work equally well and have similar side effects. However, women who have undesirable side effects while taking one AI medication may have fewer side effects with a different AI for unclear reasons.
Women who have not gone through menopause and who are not getting shots to stop the ovaries from working (see below) should not take AIs, as they do not block the effects of estrogen made by the ovaries. Often, doctors will monitor blood estrogen levels in women whose menstrual cycles have recently stopped, those whose periods stopped with chemotherapy, or those who have had a hysterectomy but their ovaries are still in place, to be sure that the ovaries are no longer producing estrogen.
- Ovarian suppression or ablation. Ovarian suppression is the use of drugs to stop the ovaries from producing estrogen. Ovarian ablation is the use of surgery to remove the ovaries. These options may be used in addition to another type of hormonal therapy for women who have not been through menopause.
- For ovarian suppression, gonadotropin or luteinizing releasing hormone (GnRH or LHRH) agonist drugs are used to stop the ovaries from making estrogen, causing temporary menopause. Goserelin (Zoladex) and leuprolide (Eligard, Lupron) are types of these drugs. Since they are not very effective for treating breast cancer on their own, they are typically given in combination with other hormonal therapy. They are given by injection every 4 weeks and stop the ovaries from making estrogen. The effects of GnRH drugs go away if treatment is stopped.
- For ovarian ablation, surgery to remove the ovaries is used to stop estrogen production. While this is permanent, it can be a good option for women who no longer want to become pregnant, especially since the cost is typically lower over the long term.
Hormonal therapy for women after menopause
Women who have gone through menopause and are prescribed hormonal therapy have several options:
- Tamoxifen for 5 to 10 years
- An AI for 5 to 10 years
- Tamoxifen for 5 years, followed by an AI for up to 5 years. This would be a total of 10 years of hormonal therapy.
- Tamoxifen for 2 to 3 years, followed by 2 to 8 years of an AI for a total of 5 to 10 years of hormonal therapy.
In general, women should expect 5 to 10 years of hormonal therapy. The tumor biomarkers and other features of the cancer may also impact who is recommended to take a longer course of hormonal therapy.
Hormonal therapy for premenopausal women
As noted above, premenopausal women should not take AI medications without ovarian suppression, as they will not lower estrogen levels. Options for adjuvant hormonal therapy for premenopausal women include the following:
- Tamoxifen for 5 years. Then, treatment is based on their risk of cancer recurrence as well as whether or not they have gone through menopause in those 5 years.
- If a woman has not gone through menopause after the first 5 years of treatment and is recommended to continue treatment, they can continue tamoxifen for another 5 years, for a total of 10 years of tamoxifen. Alternatively, a woman could start ovarian suppression and switch to taking an AI for another 5 years.
- If a woman goes through menopause during the first 5 years of treatment and is recommended to continue treatment, they can continue tamoxifen for an additional 5 years or switch to an AI for 5 more years. This would be a total of 10 years of hormonal therapy. Only women who are clearly post-menopausal should consider taking an AI.
- Ovarian suppression for 5 years along with additional hormonal therapy, such as tamoxifen or an AI, may be recommended in the following situations, depending on a woman’s age and risk of recurrence:
- For women who are diagnosed with breast cancer at a very young age.
- For women who have a high risk of cancer recurrence.
- For women with stage II or stage III cancer when chemotherapy is also recommended. However, evidence now suggests benefits independent of the use of chemotherapy as well.
- For women with stage I or stage II cancer with a higher risk of recurrence who may consider also having chemotherapy.
- For women who cannot take tamoxifen for other health reasons, such as having a history of blood clots, so they can take an AI medication.
- Ovarian suppression is not recommended in addition to another type of hormonal therapy in the following situations:
- For women with cancer that is not very likely to recur.
- For women with stage I cancer when chemotherapy has not been recommended.
هورمون درمانی برای زنان بعد از یائسگی
- تاموکسیفن برای 5 تا 10 سال
- هوش مصنوعی برای 5 تا 10 سال
- تاموکسیفن به مدت 5 سال و به دنبال آن هوش مصنوعی تا 5 سال. این در مجموع 10 سال درمان هورمونی خواهد بود.
- تاموکسیفن به مدت 2 تا 3 سال و به دنبال آن 2 تا 8 سال هوش مصنوعی برای مجموع 5 تا 10 سال درمان هورمونی.
درمان هورمونی برای زنان قبل از یائسگی
Targeted therapy is a treatment that targets the cancer’s specific genes, proteins, or the tissue environment that contributes to cancer growth and survival. These treatments are very focused and work differently than chemotherapy. This type of treatment blocks the growth and spread of cancer cells and limits damage to healthy cells.
Not all tumors have the same targets. To find the most effective treatment, your doctor may run tests to identify the genes, proteins, and other factors in your tumor. In addition, research studies continue to find out more about specific molecular targets and new treatments directed at them. Learn more about the basics of targeted treatments.
The first approved targeted therapies for breast cancer were hormonal therapies. Then, HER2-targeted therapies were approved to treat HER2-positive breast cancer.
HER2-targeted therapy (updated 10/2020)
- Trastuzumab (FDA-approved biosimilarforms are available). This drug is approved as a therapy for non-metastatic HER2-positive breast cancer. It is given either as an infusion into a vein every 1 to 3 weeks or as an injection into the skin every 3 weeks. Currently, patients with stage I to stage III breast cancer (see Stages) should receive a trastuzumab-based regimen, often including a combination of trastuzumab with chemotherapy, followed by a total of 1 year of adjuvant trastuzumab. Patients receiving trastuzumab have a small (2% to 5%) risk of heart problems. This risk is increased if a patient has other risk factors for heart disease or receives chemotherapy that also increases the risk of heart problems at the same time. These heart problems may go away and can be treated with medication.
- Pertuzumab (Perjeta).This drug is approved for stage II and stage III breast cancer in combination with trastuzumab and chemotherapy. It is given as an infusion into a vein every 3 weeks.
- Pertuzumab, trastuzumab, and hyaluronidase–zzxf (Phesgo). This combination drug, which contains pertuzumab, trastuzumab, and hyaluronidase-zzxf in a single dose, is approved for people with early-stage HER2-positive breast cancer. It may be given in combination with chemotherapy. It is given by injection under the skin and can be administered either at a treatment center or at home by a health care professional.
- Neratinib (Nerlynx).This oral drug is approved as a treatment for higher-risk HER2-positive, early-stage breast cancer. It is taken for a year, starting after patients have finished 1 year of trastuzumab.
- Ado-trastuzumab emtansine or T-DM1 (Kadcyla). This is approved for patients with early-stage breast cancer who have had treatment with trastuzumab and chemotherapy with either paclitaxel or docetaxel followed by surgery, and who had cancer remaining (or present) at the time of surgery. ASCO recommendsthat these patients receive 14 cycles of T-DM1 after surgery unless the cancer recurs or the side effects from T-DM1 become too difficult to manage. T-DM1 is a combination of trastuzumab linked to a very small amount of a strong chemotherapy. This allows the drug to deliver chemotherapy into the cancer cell while lessening the chemotherapy received by healthy cells, which usually means that it causes fewer side effects than standard chemotherapy. T-DM1 is given by vein every 3 weeks.
This information is based on the ASCO guideline, “Selection of Optimal Adjuvant Chemotherapy and Targeted Therapy for Early Breast Cancer.” Please note that this link takes you to another ASCO website.
Talk with your doctor about possible side effects of specific medications and how they can be managed.
Bone modifying drugs block bone destruction and help strengthen the bone. They may be used to prevent cancer from recurring in the bone or to treat cancer that has spread to the bone. Bone modifying drugs are not a substitute for standard anti-cancer treatments. Certain types of bone modifying drugs are also used in low doses to prevent and treat osteoporosis. Osteoporosis is the thinning of the bones.
There are 2 types of drugs that block bone destruction:
- These block the cells that destroy bone, called osteoclasts.
- Denosumab (Prolia, Xgeva).An osteoclast-targeted therapy called a RANK ligand inhibitor. ASCO does not recommend using denosumab as an adjuvant treatment to prevent breast cancer recurrence.
All people with breast cancer who have been through menopause, regardless of the cancer’s hormone receptor status and HER2 status, should have a discussion with their doctor whether bisphosphonates are right for them. Several factors affect this decision, including your risk of recurrence, the side effects of treatment, the cost of treatment, your preferences, and your overall health.
If treatment with bisphosphonates is recommended, ASCO recommends starting within 3 months after surgery or within 2 months after adjuvant chemotherapy. This may include treatment with clodronate (multiple brand names), ibandronate (Boniva), or zoledronic acid (Reclast, Zometa). Clodronate is not available in the United States.
This information is based on the ASCO and Ontario Health (Cancer Care Ontario) guideline, “Use of Adjuvant Bisphosphonates and Other Bone-Modifying Agents in Breast Cancer.” Please note that this link takes you to another ASCO website.
Other types of targeted therapy for breast cancer (updated 04/2022)
You may have other targeted therapy options for breast cancer treatment, depending on several factors. The following drugs are used for the treatment of non-metastatic breast cancer.
- Olaparib (Lynparza).This is a type of oral drug called a PARP inhibitor, which destroys cancer cells by preventing them from fixing damage to the cells. ASCO recommends using olaparib to treat early-stage, HER2-negative breast cancer in people with an inherited BRCA1 or BRCA2 gene mutation and a high risk of breast cancer recurrence. Adjuvant olaparib should be given for 1 year following the completion of chemotherapy, surgery, and radiation therapy (if needed).
- Abemaciclib (Verzenio). This oral drug, called a CDK4/6 inhibitor, targets a protein in breast cancer cells called CDK4/6, which may stimulate cancer cell growth. It is approved as treatment in combination with hormonal therapy (tamoxifen or an AI) to treat people with hormone receptor-positive, HER2-negative, early breast cancer that has spread to the lymph nodes and has a high risk of recurrence. ASCO recommendsconsideration of 2 years of treatment with abemaciclib combined with 5 or more years of hormonal therapy for patients meeting these criteria, including for people whose cancer has a Ki-67 score higher than 20% (see Diagnosis).
Many of the following drugs are used for advanced or metastatic breast cancer.
- Alpelisib (Piqray).Alpelisib is an option along with the hormonal therapy fulvestrant for people with hormone receptor-positive, HER2-negative metastatic breast cancer that has a PIK3CA gene mutation and has worsened during or after hormonal therapy.
- Drugs that target the CDK4/6 proteinin breast cancer cells, which may stimulate cancer cell growth. These drugs include abemaciclib (Verzenio), palbociclib (Ibrance), and ribociclib (Kisqali). They are approved for women with ER-positive, HER2-negative advanced or metastatic breast cancer and may be combined with some types of hormonal therapy. They may also be used in conjunction with fulvestrant in endocrine-resistant second-line disease.
- Lapatinib (Tykerb). This may be an option for women with HER2-positive advanced or metastatic breast cancer when other medications are no longer effective at controlling the cancer’s growth. It may be combined with the chemotherapy capecitabine, the hormonal therapy letrozole, or the HER2 targeted therapy trastuzumab.
- Tucatinib (Tukysa).Tucatinib, when added to capecitabine chemotherapy and trastuzumab, is approved for the treatment of advanced unresectable or metastatic HER2-positive breast cancer, including cancer that has spread to the brain, in those who have already received 1 or more HER2-targeted therapy. Unresectable means surgery is not an option. Tucatinib is a tyrosine kinase inhibitor designed to turn off HER2. It is an oral medication that is given twice daily.
- Sacituzumab govitecan-hziy (Trodelvy). The FDA has approved the use of sacituzumab govitecan-hziy for the treatment of people with metastatic triple-negative breast cancer who have already received at least 2 treatments, including 1 treatment for metastatic disease. It is also approved for people with locally advanced triple-negative breast cancer that cannot be treated with surgery. Sacituzumab govitecan-hziy is an antibody-drug conjugate, which means the antibody attaches to a cancer cell and then delivers the anticancer drug it carries to start destroying the cancer cell. Sacituzumab govitecan-hziy is given by vein, or intravenously, on days 1 and 8 of every 21-day cycle.
- Entrectinib (Rozyltrek) and larotrectinib (Vitrakvi). These may be used for breast cancer with an NTRKfusion that is metastatic or cannot be removed with surgery and has worsened with other treatments (see Diagnosis).
- This oral drug may be used for people with metastatic HER2-negative breast cancer and an inherited BRCA1 or BRCA2 gene mutation who have previously received chemotherapy. It is a type of drug called a PARP inhibitor, which destroys cancer cells by preventing them from fixing damage to the cells.
- Talazoparib (Talzenna). This may be an option for women with locally advanced or metastatic HER2-negative breast cancer and a BRCA1or BRCA2 gene mutation. It is a PARP inhibitor.

